I. Iwwersiicht iwwer d'ESMORichtlinn 2025
Am August 2025 huet d'ESMO offiziell d'Early and locally advanced non small cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up erausginn, déi an der féierender Onkologie-Zeitschrift Annals of Oncology publizéiert gouf. Dëst ass déi éischt ëmfaassend Aktualiséierung zënter der Versioun vun 2017 a bitt eng extrem autoritéit Referenz fir Onkologen weltwäit.

Lungenkriibs huet weltwäit déi héchst Inzidenz a Mortalitéit vun alle bösartege Krankheeten. All Joer gëtt et méi wéi 2,2 Millioune nei Fäll a méi wéi 1,8 Millioune Doudesfäll, wat Lungenkriibs zur heefegster Doudesursaach duerch Kriibs bei Männer a Fraen mécht. Net-klengzelleg Lungenkriibs (NSCLC) mécht ongeféier 80-85% vun alle Lungenkriibspatienten aus. Virun dësem eeschten Hannergrond bréngt d'Verëffentlechung vun der Richtlinn fir 2025 nei wëssenschaftlech Schwong an d'klinesch Praxis, woubäi d'Aktualiséierung vun de Strategien fir d'Test vu Biomarker besonnesch entscheedend ass.
II. Interpretatioun vun de wichtegsten Aktualiséierunge vun de Richtlinnen
2.1 Biomarker Tester: Vun "Optional" bis "Essential"
D'Richtlinn vun 2025 mécht eng wichteg strategesch Upassung wat d'Biomarkertester ugeet. D'Richtlinn seet explizit, datt Biomarkertester essentiell fir d'Behandlungsentscheedung bei Patienten mat NSCLC am Stadium IB-III sinn.
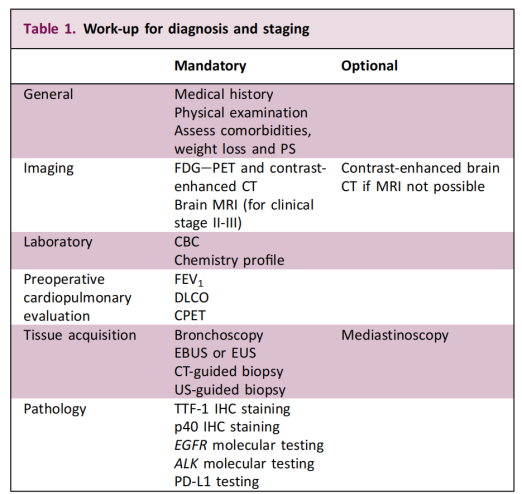
Dës Empfehlung erweidert d'molekular Tester vun hirem fréiere Fokus op Patienten mat fortgeschrattener Krankheet op Fäll am fréie Stadium, déi resektable kënne ginn. D'Haaptzil ass et, Mutatiounen am Treibergen z'identifizéieren an eng wëssenschaftlech Basis fir eng personaliséiert Präzisiounsbehandlung ze bidden. D'Richtlinn betount och, datt d'Machbarkeet vun enger Biopsie an den diagnosteschen Usaz vun engem multidisziplinäre Team op Basis vun de Charakteristike vum Patient an dem Tumor bestëmmt solle ginn.
Wat déi spezifesch Teststrategie ugeet, recommandéiert d'Richtlinn kloer, datt genetesch Tester virun der chirurgescher Entscheedung duerchgefouert ginn, an datt se op d'mannst EGFR an ALK ofdecken. Dëst Konzept vum "Test am Viraus" huet eng grouss klinesch Bedeitung fir déi präzis Stratifikatioun an déi personaliséiert Behandlung vun NSCLC am fréie Stadium - d'Aktualitéit an d'Genauegkeet vun den Testergebnisse bestëmmen direkt d'Wiel vun der spéiderer adjuvanter Therapie.
2.2 Therapeutesch Duerchbréch bei Driver-Onkogen-positiver NSCLC am fréie Stadium
D'Richtlinn vun 2025 integréiert Beweiser aus verschiddene grousse klineschen Studien, fir e kloere präzise Behandlungswee fir Patienten mat Driver-Onkogen-positiver NSCLC am fréie Stadium ze etabléieren.
EGFR-mutéiert positiv Patienten:Baséierend op der wichteger ADAURA-Studie ass postoperativ adjuvant Osimertinib fir dräi Joer zum globale Standard vun der Behandlung fir Patienten mat EGFR Exon 19-Deletiounen oder Exon 21 L858R-Mutatiounen ginn. D'ADAURA-Studie ass eng international, multizentresch, randomiséiert, kontrolléiert Phase-III-Studie, déi d'Effizienz a Sécherheet vum adjuvanten Osimertinib bei Patienten mat komplett resektéiertem Stadium IB-IIIA EGFR-mutéierten NSCLC evaluéiert. D'Studie huet gewisen, datt Osimertinib souwuel d'krankheetsfräi Iwwerliewe wéi och d'Gesamtiwwerliewe am Verglach mam Placebo däitlech verbessert huet, wouduerch Osimertinib als neie Standard vun der Behandlung fir dës Populatioun etabléiert gouf. Exploratoresch Analysen vun der ADAURA-Studie hunn awer ugedeit, datt ongeféier 36% vun den fréizäitegen Ofsetzunge vun der Behandlung duerch Niewewierkungen verursaacht goufen, an weider 31% op eng Entscheedung vum Patient zeréckzeféieren waren. Dëst Resultat ënnersträicht d'Noutwennegkeet vu präzise Baseline-Tester virun der Behandlung, fir sécherzestellen, datt eng gezielte Therapie u Patienten ginn gëtt, déi e laangfristege Virdeel dovunner kënne kréien.
ALK-positiv Patienten:Baséierend op der ALINA-Studie ass postoperativ adjuvant Alectinib fir zwee Joer elo de Standard vun der Behandlung. An der Primäranalyse vun der Phase-III randomiséierter Open-Label ALINA-Studie huet Alectinib e markanten krankheetsfräien Iwwerliewensvirdeel an der Stadium II-IIIA-Populatioun gewisen, mat engem Hazard Ratio vun 0,24. Aktualiséiert Donnéeën aus der ALINA-Studie, déi um ESMO 2025 Kongress presentéiert goufen, hunn gewisen, datt no ≥3 Joer Follow-up de DFS-Virdeel vun Alectinib "nohalteg a klinesch sënnvoll" bliwwen ass, mat engem Hazard Ratio vun 0,36 an der Stadium II-IIIA-Populatioun. Déi lescht gemellt 4-Joer Gesamtiwwerliewensquote huet 98,4% erreecht, d'4-Joer DFS-Quote louch bei 75,5%, an den DFS vum Zentralnervensystem war och verbessert, ouni nei Sécherheetssignaler. Dës robust Donnéeën etabléieren adjuvant Alectinib weider als Standard vun der Behandlung no der Resektioun vun ALK-positiven NSCLC a ënnersträichen de Wäert vu präzisen Tester fir sou Patienten z'identifizéieren.
Wiel vun der Testmethod:D'ESMO-Richtlinn vun 2025 nennt explizitMultiplex RT-PCR Panel Testernieft RNA-baséierten NGS, IHC a FISH als ee vun den empfohlenen techneschen Approche fir d'ALK-Fusiounsdetektioun. Dëst weist drop hin, datt d'Haaptfuerderung vun der Richtlinn ass, Tester duerchzeféieren, fir klinesch Entscheedungen ze leeden, anstatt eng spezifesch Testplattform ze verlaangen. Fir RT-PCR-Produkter, déi sech op d'EGFR- an ALK-Detektioun konzentréieren, bitt dës flexibel Teststrategie eng staark, op de Richtlinne baséiert Begrënnung fir hir Notzung an der klinescher Praxis.
III. Technesch Léisunge fir Präzisiounstester
D'Richtlinn vun 2025 réckelt d'Tester an d'Entscheedungsphase virun der Operatioun, wat d'Messlat fir d'Genauegkeet, d'Sensibilitéit an d'Zougänglechkeet vun den Tester erhéicht. Déi zwee RT-PCR-baséiert Detektiounsprodukter, déi hei ënnendrënner beschriwwe ginn, entspriechen den Ufuerderunge vun der Richtlinn aus technescher Siicht genee.
3.1 EGFR Mutatiounsdetektiounskit – Verbessert ARMS Technologieplattform
KärtechnologieVerbessert ARMS Technologie erméiglecht eng spezifesch Amplifikatioun vu Mutantsequenzen mat gerénger Abundanz géint en Hannergrond mat héijem Wildtyp
Dräi technesch Sécherheetsmoossnamen:
-Verbessert ARMS → verbessert Mutatiounserkennung
-Enzymatesch Anreicherung → verdaut Wildtyp-Hannergrond a beräichert Mutantsequenzen
-Temperaturblockéierung → ënnerdréckt net spezifesch Amplifikatioun
LeeschtungEmpfindlechkeet vun1% Mutant-Allelfrequenz
KontaminatiounskontrollIntegréiert intern Kontroll + UNG-Enzym verhënnert Kontaminatioun
ËmdréizäitZougemaachent Réierbetrieb, ongeféier120 Minutten
Kompatibilitéit vu Beispiller:Gewief/flësseg BiopsieBeispiller → adresséiert d'Ufuerderung "am Viraus testen"
Ofdeckung:45 Mutatiounenan EGFR Exonen 18-21, präzis iwwereneestëmmend mat de Richtlinn-markéierte Regiounen (Exon 19 Deletiounen an Exon 21 L858R)
Klinesch BenotzungLeet direkt d'EGFR-TKI Therapie
3.2 MMT EML4-ALK Fusiounsdetektiounskit – RNA-baséiert Fusiounsdetektiounsléisung

-TechnologieplattformRNA-baséiert RT-PCR – bitt inherent Virdeeler géintiwwer DNA-baséierte Methoden fir d'Fusiounsdetektioun
-RNA-baséiert VirdeelDetektéiert direkt expriméiert Fusiounstranskripten, wouduerch falsch Negativer effektiv vermeit ginn.
-StudienbeweiserBei ALK-Fusioune mat gerénger Abundanz ass RT-PCR däitlech méi zouverlässeg wéi DNA-baséiert Tester.
-Sensibilitéit: Detektéiert Fusiounen bis op20 Kopien pro Reaktioun
-Ofdeckung vu Varianten: Coveren12 üblech EML4-ALK Fusiounsvarianten(inklusiv Variant 1 ~33%; Varianten 3a/3b zesummen ~29%)
-Operatioun & KontaminatiounskontrollZougemaacht Röhrchen, ~120 Minutten; agebaute Prozesskontrollen + UNG-Enzym verhënneren falsch Resultater
-InstrumentenkompatibilitéitKompatibel mat verschiddenen üblechen Echtzäit-PCR-Instrumenter
-Ausriichtung vun de RichtlinnenEntsprécht ganz gutt der ESMO-Richtlinn
IV. Konsistenz tëscht den Tester an den Empfehlungen vun de Richtlinnen
Déi zwee Detektiounsprodukter entspriechen héich der ESMO 2025 Richtlinn fir fréi a lokal fortgeschratt net-klengzelleg Lungenkrebs a folgende Schlësseldimensiounen:
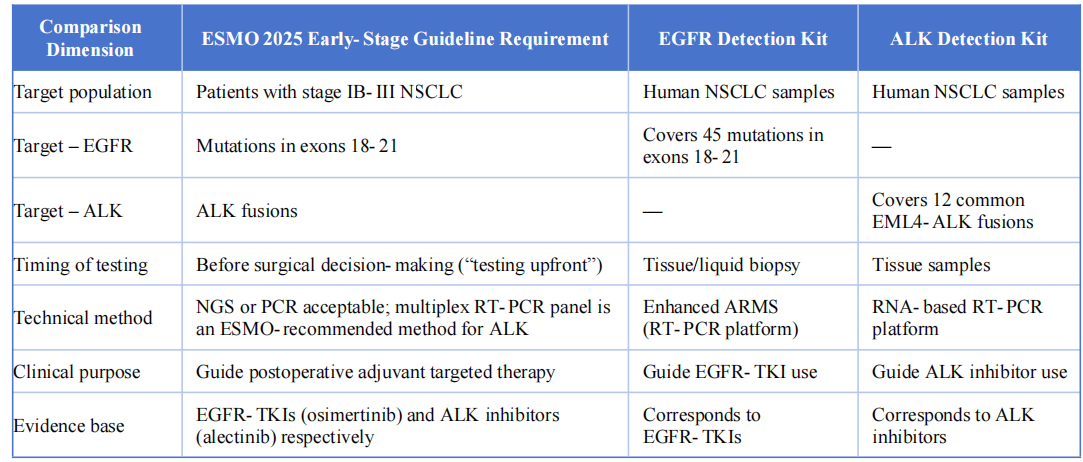
V. Schlussfolgerung
D'ESMO 2025 Richtlinn fir fréi Stadium NSCLC féiert eng nei Ära vun der Präzisiounsdiagnos a Behandlung an, déi sech op "Tester am Viraus, präzis Zilsetzung an Optimiséierung vun der Behandlung.Den EGFR Mutatiounsdetektiounskit an den MMT EML4-ALK Fusiounsdetektiounskit erfëllen d'Ufuerderunge vun der Richtlinn a punkto Ziler, Timing a Genauegkeet duerch ënnerschiddlech technesch Weeër.
Den EGFR-Kit benotzt eng verbessert ARMS-Technologie fir d'héichsensibel Detektioun vu gezielte Mutatiounen a limitéierte Proben, andeems en souwuel Gewebe- wéi och Flëssegkeetsbiopsie ënnerstëtzt, fir "Tester am Viraus" z'erméiglechen.
Den ALK-Kit baséiert op RNA-baséierter RT-PCR a bitt Virdeeler géintiwwer DNA-Methoden fir d'Fusiounsdetektioun, wat mat der Empfehlung vun ESMO fir Multiplex-RT-PCR-Paneele fir ALK-Tester iwwereneestëmmt.
Zesummen bilden dës zwee Produkter eng Präzisiounstestléisung, déi der ESMO 2025-Richtlinn entsprécht a personaliséiert adjuvant Therapie fir NSCLC am fréie Stadium ënnerstëtzt.
Referenzen:
- Zer A, Ahn MJ, Barlesi F, et al. Fréi a lokal fortgeschratt net-klengzelleg Lungenkrebs: ESMO Clinical Practice Guideline fir Diagnos, Behandlung a Follow-up. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Zäitpunkt vun der Verëffentlechung: 06. Mee 2026

